Опасность для человека и природы
Как и другие галогены хлор способен наносить вред человеку. Этот газ, будучи сильным окислителем, способен к образованию кислот при контакте с влагой воздуха. Эта особенность оказывает поражающее воздействие на лёгочную ткань живых существ, вызывая сильные химические ожоги. Это свойство хлора было применено Германией в начале 20-го века во время Первой мировой войны, где этот газ, наряду с некоторыми другими, использовался в качестве боевого отравляющего вещества.
Поскольку вода входит в состав всех живых клеток и является неотъемлемой частью биосферы, образование кислот хлора может наносить урон не только людям, но и всем живым существам.
Ещё одно важное свойство хлора – его участие в ионно-солевом обмене живых организмов. Этот биогенный элемент присутствует во всех живых организмах, включая растения, и его наличие крайне важно для правильного существования
Превышение концентрации хлорид-ионов приводит к множественным нарушениям в нормально ионно-солевом обмене, поддержании осмотического давления клеток, что приводит к их гибели и ухудшению общего состояния организма.
Существуют организмы-экстремофилы, которые могут существовать в условиях с высокой концентрацией хлора в окружающей среде – галофилы. Галофилы-растения называются галофитами, а галофилы-бактерии – галобактериями.
Похожие новости
11/02/2021
Российские и французские ученые к 2022 году впервые изучат влияние ветров на загрязнение территорий Сибири и Арктики тяжелыми металлам, для этого будут отобраны и исследованы пробы снега, воды и лишайников от Томской области до Ямала, сообщил ТАСС участник проекта, директор Центра коллективного пользования “Мегапрофиль” научного управления Томского госуниверситета (ТГУ) Сергей Воробьев.
521
03/07/2020
Программа мегагрантов была запущена в 2010 году. Она подразумевает международное сотрудничество российских вузов и научных организаций с ведущими зарубежными учеными и научно-образовательными центрами в сферах науки, образования и инноваций.
3188
03/03/2021
Молодой ученый химического факультета Томского госуниверситета Олеся Лапуть работает над созданием материала, способствующего ускорению регенерации повреждённых кожных покровов. Основным инструментом для достижения этой цели выступает обработка потоками низкотемпературной плазмы, модифицирующей поверхность импланта.
846
10/03/2021
Ученые лаборатории радиофизических и оптических методов изучения окружающей среды РФФ ТГУ нашли способ определять загрязнения водоемов по планктону. Основной инструмент – цифровая голографическая камера.
605
27/11/2020
25 ноября открылась международная онлайн-конференция «Хронодиагностика и хронотерапия: основы цифрового здоровья». Организатором прямой трансляции выступил Тюменский государственный медицинский университет.
1435
25/03/2021
Российский фонд фундаментальных исследований и Государственный фонд естественных наук Китая поддержат создание препаратов от коронавируса на основе «Триазавирина». Группа ученых под руководством профессора кафедры органической и биомолекулярной химии УрФУ, директора Института органического синтеза им.
537
15/02/2021
План проведения в 2021-м Года науки и технологий сформирован исходя из национальных целей развития России до 2030 года, сообщил глава Минобрнауки Валерий Фальков. Он представил план на первом заседании оргкомитета по проведению тематического года, сообщили в понедельник в аппарате зампредседателя правительства РФ Дмитрия Чернышенко.
777
29/12/2020
Директор Инженерной школы природных ресурсов ТПУ Наталья Гусева поделилась результатами, которых достиг коллектив школы в 2020 году, и рассказала о целях и задачах на будущий год. Уходящий год стал точкой отсчета новой реальности для всего мира, и, чтобы в нее «встроиться», нам пришлось многое пересмотреть и изменить в своей деятельности.
2005
15/12/2020
Полученные результаты помогут осуществлять контроль качества озонового слоя, который участвует в формировании атмосферы и климата Земли, влияет на качество воздуха, охраняет планету от жесткого ультрафиолетового излучения.
773
Хлориды – что это?
Хлориды – это «собрание» химических веществ, похожие свойства которых обусловлены присутствием хлорид-иона (Cl—). Яркие представители этого ряда:
- NaCl – хлористый натрий. Всем известная пищевая поваренная и морская соль.
- AgCl – хлорид серебра. Главный источник антимикробных ионов. Аллерген – раздражает кожу и слизистую глаз.
- HgCl2 – хлористая ртуть (сулема). В незначительных количествах отменный дезинфектор, но также ядовитый, может нести угрозу человеку.
- Hg2Cl2 – хлорид одновалентной ртути. В обиходе известен как каломель, довольно эффективное слабительное средство.
- KCl – калия хлорид. Частая основа калийных удобрений. В медицине востребован в роли биодобавки – помогает при кардиологических патологиях.
- BaCl2 – хлористый барий. Содержится в составе инсектицидных препаратов, борющихся со зловредными насекомыми. Для человека тоже токсичен в высоких концентрациях.
- CaCl2 – хлорид кальция. Используется в качестве пищевой добавки. Также служит отвердителем-эмульгатором.
- MgCl2 – магниевая соль соляной кислоты. Вопреки использованию в пищевой промышленности в роли добавки, в меру агрессивна (3-й класс опасности по классификации), причина коррозионных разрушений.
Во всех видах воды – от бутилированной, специально очищенной питьевой до сточной формации – хлориды непременно присутствуют. Определение концентрации хлорид-иона (Cl—) строго обязательно для всех типов жидкостей, которые могут применяться в качестве питьевых источников, использоваться в технологических процессах, «выделяться» в виде канализационных стоков.
Общие сведения
Содержание ионов Cl— в воде и их определение регламентировано нормативными и санитарными документами:
- Технический регламент Евразийского экономического союза ТР ЕАЭС 044/2017 «О безопасности упакованной питьевой воды, включая природную минеральную воду».
- СанПиН 2.1.4.1116-02 «Питьевая вода. Гигиенические требования к качеству воды, расфасованной в емкости. Контроль качества».
- СанПиН 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества. Гигиенические требования к обеспечению безопасности систем горячего водоснабжения».
- СанПиН 2.1.4.1175-02 «Гигиенические требования к качеству воды нецентрализованного водоснабжения. Санитарная охрана источников».
- СанПиН 2.1.5.980-00 «Гигиенические требования к охране поверхностных вод».
- СанПиН 2.1.7.573-96 «Гигиенические требования к использованию сточных вод и их осадков для орошения и удобрения».
- Межгосударственный стандарт ГОСТ 4245-72 «Методы определения содержания хлоридов.
Важное, но вместе с тем и опасное для потребителей физическое свойство хлоридов – высокая способность к растворению в воде при обычных условиях без нагревания. При контакте с водной средой хлориды участвуют в необратимом гидролизе, способствуя образованию соляной кислоты. Хлороводородная кислота вместе со своими солями портит органолептические характеристики воды (мутность, цветность, запах, вкус), участвует в коррозии металлических деталей оборудования и водопроводных труб, создаёт накипь в котлах и чайниках
Хлороводородная кислота вместе со своими солями портит органолептические характеристики воды (мутность, цветность, запах, вкус), участвует в коррозии металлических деталей оборудования и водопроводных труб, создаёт накипь в котлах и чайниках.
Сточные и природные воды
Круговорот солей соляной кислоты в природе и в быту – неизбежный процесс. Хозяйственные нужды, медицина, пищевая отрасль без участия хлоридов будут испытывать дефицит в нужных химических компонентах.
Нормальная концентрация хлоридов в пресных озерах и реках обычно колеблется от сотых долей до нескольких граммов, число анионов Cl— в морях и океанах чаще всего достигает 87% от общего числа анионов других кислот и солей. В природном круговороте веществ активно задействованы грунтовые и поверхностные воды. В жаркую погоду, испаряясь с водой, хлориды попадают на небо, откуда проливаются дождями на землю, попадая туда, где их не было. Во время этого процесса их естественная концентрация в водоемах возрастает.
Воспользовавшись природными водными запасами, человек решает свои насущные проблемы. Еще больше загрязняя живительную влагу, окончательно превращает ее в сточный «субстрат», который зачастую очистить уже не представляется возможным. Чтобы результаты такой деятельности не переходили все мыслимые и немыслимые границы, санитарные службы установили ПДК (предельно допустимые количества) по содержанию хлоридов в разных типах воды.
Наиболее востребованные наборы
Лидеры рейтинга — комплекты, выполняющие распространенные задачи, обладающие необходимой точностью и приемлемой ценой:
- Комплект, состоящий из pH-метра и солемера, предлагает фирма Lizi (Китай). Набор предназначен для бытового применения. Оба прибора компактные, автономные. Цена комплекта около 3 500 руб.
- Фирма Watertest продает набор, состоящий из электролизера, измерителей pH, TDS, ОВП. Продавцы считают, что комплект полностью покрывает потребности по исследованию качества воды в быту и на предприятиях общественного питания. Цена набора около 5 000руб.
- Набор PHCOM от фирмы HM Digital (Корея). Позволяет измерить кислотность, минерализацию, электропроводность, температуру исследуемого раствора. В набор входит 2 прибора: pH-метр и солемер. Изготовители характеризуют их как устройства профессионального уровня. Цена набора несколько превышает 10 000 руб.
Методы удаления хлоридов из воды
Избыток хлоридов искажает вкус питьевой воды, а многие технологические процессы не допускают использование хлорированной воды, поэтому ее подвергают дехлорированию.
Простые способы
В быту хлор из воды удаляют следующими способами:
Слив застоявшейся в трубах воды. Вечером, когда происходит максимальный водозабор, есть смысл набрать 5-10 литров впрок. Отстаивание. В быту частично удалить хлор можно, если воду из-под крана налить в широкую емкость, к примеру, кастрюлю, и дать отстояться 3-4 часа
Воду важно перемешивать время от времени, иначе газообразный хлор удаляется только с 1/3 глубины емкости. Кипячение
Важно помнить, что при кипячении улетучивается только газообразный хлор. Перекристаллизация
Суть техники заключается в разной скорости замерзания воды с примесями и чистой воды. Воду несколько раз замораживают и размораживают.
Трудоемкие и малоэффективные бытовые способы дехлорирования с успехом заменяет качественная фильтрующая система, встроенная в водопроводную систему дома или квартиры.
Промышленные
В настоящее время распространены следующие промышленные способы дехлорирования:
- озонирование;
- сорбционный метод;
- ионный обмен;
- обратный осмос.
| Метод очистки | Суть процесса | Недостаткидостоинства метода |
| Озонирование | Под воздействием сильного окислителя хлориды переходят в нерастворимые формы и путем механической фильтрации удаляются из воды. | · озонаторы подходят только для промышленного использования и на водоочистительных станциях; · высокая стоимость; · требуют постоянного контроля. |
| Сорбция | Хлориды задерживаются фильтром из активированного угля с повышенной сорбирующей способностью. | · из-за бурного роста бактерий на активированном угле воду необходимо предварительно обеззаразить. |
| Ионный обмен | Наполнитель из ионообменной смолы поглощает отрицательно заряженные соли, в том числе и хлориды. | · обязателен тщательный контроль процесса; · метод не подходит для бытового использования. |
| Обратный осмос | Удаление хлоридов достигает 99,5%. Полупроницаемая мембрана задерживает хлориды, обессоленная вода поступает к потребителю. | · компактность установки; · длительная эксплуатация; · установка в домах и на производстве; · на степень очистки исходный состав воды не влияет; · снижается не только жесткость, но и показатель цветности, концентрация железа. Исчезает специфический запах. |
Из таблицы видно, что система обратного осмоса наиболее эффективна и универсальна. Установка обратного осмоса в квартире, коттедже или на предприятии способна уменьшить концентрацию хлоридов до нормального уровня, сделав ее пригодной для питья.
Контроль за качеством воды позволяет сохранить здоровье живых существ, оптимизировать технические процессы, позаботиться об экологии.
Предсказание климатических моделей
В ходе исследования, участие в котором приняли ученые из университетов Белой Розы Йорка, Лидса и Шеффилда, были проанализированы различные концентрации уровня CO2 в земной атмосфере. Для оценки воздействия на климат, экосистемы и производство продуктов питания, исследователи использовали широко применяемую климатическую модель, которая позволила предсказать состояние планеты вплоть до 2500 года.
Авторы работы также смоделировали распределение растительности и условия выращивания основных сельскохозяйственных культур. Это позволило им получить представление о том, к каким экологическим проблемам, возможно, придется адаптироваться начиная с 22 века и далее. Результаты моделирования также показали, что если дальнейшие усилия по борьбе с изменением климата будут равноценны сегодняшним, средние глобальные температуры продолжат расти и после 2100 года.
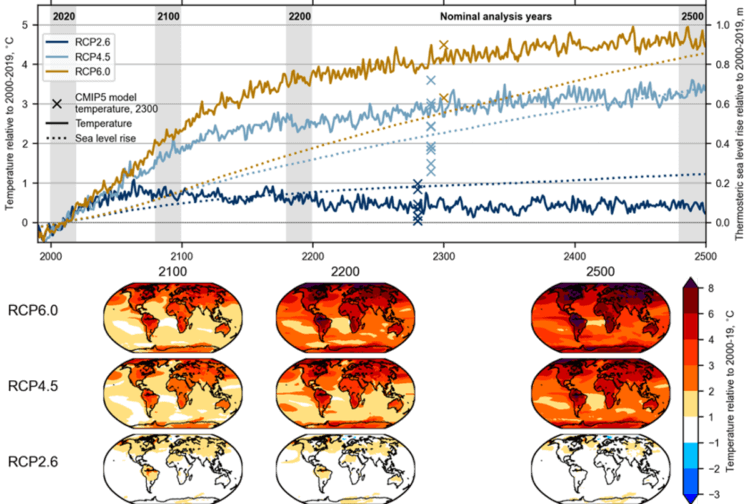
Глобальная средняя температура воздуха (сплошные линии) и аномалии повышения уровня моря (пунктирные линии) относительно среднего значения 2000-19гг. для сценариев RCP6.0, RCP4.5 и RCP2.6. Заштрихованные области выделяют интересующие временные горизонты. На нижней панели показаны пространственные аномалии относительно среднего значения 2000-19гг. для климатических условий 2100, 2200 и 2500 в рамках трех RCP.
В соответствии с этими сценариями растительность и подходящие для выращивания сельскохозяйственных культур районы переместятся к полюсам, а площадь, пригодная для некоторых культур, значительно сократится. Кроме того, исследование показало, что рост температур может оказаться смертельными для жителей тропических регионов, которые сегодня густо заселены. Эти районы могут стать непригодными для жизни.
Авторы научной работы также отмечают, что изменение климата не прекратится в ближайшие десятилетия и призывают к адаптации социально-политических и экономических систем в соответствие с решением климатических проблем – как краткосрочных, так и долгосрочных.
Методические указания на фотометрическое определение хлора в воздухе (первый метод)
УТВЕРЖДЕНЫ Заместителем Главного государственного санитарного врача СССР А.И.Заиченко 18 апреля 1977 года N 1644-77
I. Общая часть
1. Определение основано на иодкрахмальной реакции.
2. Предел обнаружения 0,25 мкг хлора в анализируемом объеме раствора.
3. Предел обнаружения в воздухе 0,5 мг/м (расчетная).
4. Определению мешают бром, фтор и иод.
5. Предельно допустимая концентрация хлора в воздухе 1 мг/м.
II. Реактивы и аппаратура
6. Применяемые реактивы и растворы.
Иод, 0,01 н. раствор (фиксанал), МРТУ 6-09-1678-64.
Стандартный раствор с содержанием 0,0178 мг/мл иода готовят в день анализа в мерной колбе емкостью 50 мл путем разведения 0,7 мл 0,01 н. раствора иода 2,5%-ным раствором иодистого калия. 1 мл стандартного раствора соответствует 5 мкг хлора.
Калий иодистый, ГОСТ 4232-65, 2,5%-ный раствор.
Ртуть двуиодистая, ГОСТ 3206-46.
Крахмал растворимый, ГОСТ 10163-62, 0,2%-ный раствор. 2 г растворимого крахмала и 10 мг двуиодистой ртути растирают с 10 мл воды. Полученную суспензию медленно вливают в 1 л кипящей воды. Кипячение продолжают пока раствор не станет прозрачным. По охлаждении сливают в бутыль с пришлифованной пробкой; раствор хранится до заметного помутнения.
Поглотительный раствор — смешивают 100 мл 2,5%-ный раствор иодида калия с 50 мл 0,2%-ного раствора крахмала и кипятят 2-3 мин. По охлаждении раствор разбавляют водой до 500 мл. Раствор можно хранить в течение 7 дней в бутыли с пришлифованной пробкой.
7. Применяемые посуда и приборы.
Аспирационное устройство.
Поглотительные приборы Зайцева (см. рис.9).
Колбы мерные, ГОСТ 1770-74, вместимостью 1 л, 500 мл и 50 мл.
Пипетки, ГОСТ 20292-74, вместимостью 1 и 5 мл с делениями на 0,01 и 0,1 мл.
Ступка с пестиком.
Фотоэлектроколориметр.
III. Отбор пробы воздуха
8. Воздух со скоростью 0,5 л/мин аспирируют через два последовательно соединенных поглотительных прибора Зайцева, содержащих по 4 мл поглотительного раствора. Для определения 1/2 ПДК достаточно отобрать 2-3 л воздуха.
IV. Описание определения
9. Содержимое каждого поглотительного прибора переносят в кювету с толщиной слоя 1 см и фотометрируют при длине волны 574 нм по сравнению с контролем. Количество хлора определяют по предварительно построенному калибровочному графику. Для построения калибровочного графика готовят шкалу стандартов согласно табл.35.
Таблица 35
Шкала стандартов
N стандарта | Стандартный раствор, мл | 2,5%-ный раствор иодистого калия, мл | Поглотительный раствор, мл | хлора, мкг |
1 | 2,0 | 2,0 | ||
2 | 0,05 | 1,95 | 2,0 | 0,25 |
3 | 0,1 | 1,9 | 2,0 | 0,50 |
4 | 0,2 | 1,8 | 2,0 | 1,0 |
5 | 0,4 | 1,6 | 2,0 | 2,0 |
6 | 0,8 | 1,2 | 2,0 | 4,0 |
7 | 1,2 | 0,8 | 2,0 | 6,0 |
Концентрацию хлора в мг/м воздуха вычисляют по формуле:
,
где — количество хлора, найденное в пробе, мкг;
— объем воздуха, взятый для анализа и приведенный к стандартным условиям по формуле (см. приложение), л.
Текст документа сверен по: / Минздрав СССР. Методические указания на определение вредных веществ в воздухе.
Вып.1-5. — М.: ЦРИА «Морфлот», 1981
Хлор – что это за элемент?
Хлор – химический элемент группы галогенов. В нормальных условиях он выглядит, как ядовитый газ желтовато-зеленого цвета с резким запахом. Благодаря своей реакционной способности и склонности к окислению других веществ, хлор широко используется для отбеливания тканей, обеззараживания воды.
Область применения
Хлор используется для отбеливания и обеззараживания, однако, на этом его полезные свойства не ограничиваются. Этот газ имеет большое значение в различных отраслях промышленности: металлургической, полимерной, аграрной. Например, в полимерной промышленности хлор применяют для производства пластика (поливинилхлорида), технологических добавок для резин вроде хлорпарафина ХП-470 А. Эта добавка массово используется в производстве резинотехнических изделий антипирена и ингибитора горения.
Свободный хлор
Понятие «свободный хлор» имеет широкую трактовку. Общеустановленного толкования терминов, связанных с хлором по отношению к воде, нет. В СанПиН и ГОСТ 18190-72 (методика йодометрического титрования) свободным остаточным хлором называют ту его часть, которая присутствует в воде в виде хлорноватистой кислоты, ионов её солей (гипохлоритов) или растворённого молекулярного хлора.
Активный хлор, который по определениям СанПиН и ГОСТ не является свободным, может таким считаться в повседневном общении. Активным хлором называют равновесную концентрацию хлорноватистой кислоты в исследуемой пробе.
Связанный хлор
Связанным или «связанным остаточным хлором» называют ту часть хлора, которая находится в исследуемой пробе в форме органических и неорганических хлораминов – веществ общего состава NH3-nnCln и R-NH2-nnCln. Хлорамины, как и хлорноватистая кислота, являются обеззараживающими и окисляющими агентами, – их активность на несколько порядков ниже, – поэтому их применение весьма ограничено и не считается целесообразным. Часть хлорноватистой кислоты в условиях, подразумевающих водопользование, сама по себе переходит в хлорамины, чем и обусловлено её присутствие в большинстве проб вод, содержащих хлор.
Переход хлора из одной формы в другую в водоёмах и трубопроводах – комплексный физико-химический процесс, тяжело поддающийся описанию. Эта способность хлора к переходу из одной формы в другие связана с его высокой реакционной способностью.
Наборы приборов
Набор приборов — это мини-лаборатория, на 100% отвечающая задачам пользователя.
Сфера применения диктует рациональный состав набора:
- в быту, пищевой промышленности, при разведении рыб в первую очередь нужна информация о кислотности и минерализации воды;
- при выяснении оздоровительных возможностей воды кроме измерителей pH и TDS в набор включают ОВП-метр;
- моментальную качественную оценку водного раствора дают электролизеры. Их добавляют в набор, чтобы сделать его универсальным.
Приборы, приобретенные в комплекте, обходятся дешевле, чем те же устройства, купленные поодиночке.
Оборудование для лабораторных исследований
Большая часть оборудования, работающая в лабораториях, действуют по тем же принципам, что и приборы для частного применения. Но их возможности шире, а точность выше.
Лабораторное оборудование охватывает области недоступные непрофессиональным устройствам. Например, проводит бактериологические, санитарные исследования образцов воды.
Для химической проверки
 В лабораториях при химическом анализе воды используют фотометры. Но в более сложном варианте, чем при непрофессиональных исследованиях.
В лабораториях при химическом анализе воды используют фотометры. Но в более сложном варианте, чем при непрофессиональных исследованиях.
Пример: пламенный фотометр модели ФПА-2-01.
Это оборудование анализирует пламя с впрыснутым в него исследуемым раствором. Прибор позволяет точно ответить на вопросы о содержании в водном растворе ионов металлов (щелочных и щелочноземельных).
Инструменты для санитарно-бактериологического и микробиологического теста
Санитарно-бактериологический анализ воды заключается в обнаружении и определении концентрации вредоносных бактерий, микроорганизмов (например, кишечной палочки). Исследование проводится с использованием типового микробиологического оборудования.
Одно из немногих устройств, частично облегчающее бактериологический анализ воды — счетчик автоматического подсчета колоний бактерий ULAB UT-5502. Прибор изготовлен в Китае. Снабжен цифровой индикацией, жидкокристаллическим дисплеем.
Для радиологической проверки
В воде возможно присутствие радиоактивных элементов, в частности, газа радона. Дозиметрические исследования проводят с помощью стандартных радиометров.
Для получения данных о концентрации в воде радона и торона (радона-220) используют приборы типа Альфарад Плюс РП. Это цифровой радиометр радона и торона. Прибор способен мониторить объемную активность радиоактивных элементов в воде и других средах.
Оборудование для физико-химических тестов
Лабораторные приборы умеют устанавливать несколько физико-химических показателей в процессе одного измерения. Create MPS-1400 — типичный представитель этого класса устройств.
Create MPS-1400 — прибор лабораторный, но не стационарный. Он выполняет исследования при погружении в воду.
При этом, кроме основных физико-химических показаний (pH, температура, редокс-потенциал и так далее), умеет измерять:
- количество растворенного кислорода;
- глубину на которой находится;
- давление.
Для спектрального исследования
 Спектральные приборы — лабораторное оборудование, способное определить состав любого вещества.
Спектральные приборы — лабораторное оборудование, способное определить состав любого вещества.
Для исследования качества воды созданы специализированные спектрометры.
Спектрофотометр Lovibond SpectroDirect разработан для анализа воды различного происхождения (питьевой, технической, сточной).
С помощью прибора реализуются отечественные и зарубежные методики определения качества воды. 50 из них запрограммированы и не требуют калибровки прибора. При проведении измерений используются реагенты, разработанные фирмой Lovibond.
Сточные и природные воды
Хлор в том или ином виде присутствует во всех поверхностных водоёмах планеты. Бессточные водоёмы, такие как моря, океаны, а также некоторые озёра (Баскунчак, Иссык-Куль, Каспийское море) имеют более высокое содержание хлора. Это обусловлено природным круговоротом воды. Имеющие стоки озёра постоянно обновляют воду, содержащуюся в них, когда как бессточные водоёмы только получают воду, в которой растворены различные соединения хлора. При дальнейшем испарении воды и выпадении её в виде осадков на поверхность земли, происходит процесс вымывания хлора и его переноса в сточные водоёмы, откуда вода затем поступает в бессточные водоёмы через систему рек. Этот процесс идёт постоянно на протяжении тысяч лет, что и приводит к постепенному повышению концентрации хлоридов в воде в бессточных водоёмах. Человеческое вмешательство может привести к катастрофическим последствиям.
Пример последствий подобного рода – высыхание Аральского моря. Использование вод, питающих это бессточное озеро, рек Амударьи и Сырдарьи для орошения посевных культур Средней Азии началось в 1930-х годах. Оно привело к постепенному высыханию Арала. До падения уровня воды, это озеро было четвёртым самым крупным по площади озером мира. Его территория равнялась 68 тысячам квадратных километров. Его глубина достигала 68 метров. По состоянию на начало 2000-х годов площадь поверхности воды Аральского моря составляла лишь четверть от первоначальной, а максимальная глубина упала до 31 метра.
Другие примеры – применение хлора для обеззараживания водопроводной воды, использование хлорных отбеливателей и моющих средств для бытовых нужд и прочее. Эти виды деятельности человека – причина повышенной концентрации соединений хлора в сточных водах.
Преимущества наших датчиков хлора
Мы являемся официальными дилерами европейского завода-изготовителя и занимаемся поставками датчиков
хлора и станций дозирования, укомплектованных датчиками различного типа. Мы выбрали самые надежные
модели, которые измеряют различные хлористые соединения в жидкости.
Ключевыми преимуществами наших датчиков хлора являются:
- простое и недорогое обслуживание;
- электролит в комплекте;
- широкий диапазон измерения хлора: от 4 до 12 pH;
- возможность использования при высоком противодавлении;
- высокая точность и скорость измерения.
Для датчиков хлора также имеется большой выбор соединительных кабелей. Вы можете выбрать подходящий
кабель по своим потребностям и требованиям. Длина кабеля может составлять от 0,7 до 25 метров.
Также, если ваши датчики хлора вышли из строя, Вы можете подобрать к ним расходные части такие, как
запасные мембраны, специальные шарики и электролиты.
Специальное предложение
Выбираете датчики и комплектующие для систем дозирования и водоподготовки? Получите индивидуальное коммерческое предложение, заполнив форму.
Также проектируем и производим системы дозирования и водоподготовки в соответствии с вашим техническим заданием и/или на основе выбранного оборудования и комплектующих.
Самостоятельный тест в быту
Приборы позволяют непрофессионалу самостоятельно получить информацию о качестве воды, которой он пользуется.
Из-под крана
Для получения общих сведений о наличии примесей в водопроводной воде достаточно приобрести TDS-метр. Например, TDS-3 (о нем рассказано в этой статье). При концентрации примесей ниже 100 мг/л воду можно считать пригодной для хозяйственных нужд, умывания, приготовления пищи.
Бутилированной
Такую воду пьют, считая ее гарантированно чистой.
Чтобы уверенность в чистоте была полной нужно сделать анализ бутилированной воды, для этого желательно иметь 3 аппарата:
- TDS;
- pH;
- ОВП.
Минимальная концентрация примесей, нормальная кислотность и отрицательный ОВП сделают употребление бутилированной воды приятным и полезным.
Из родника, скважины, колодца
О наличии в исходной воде нерастворимых частиц сообщит мутномер. Его показания упростят выбор фильтра для предварительной очистки воды.
Более точный тест воды из колодца или скважины проводится с помощью солемера и pH-метра. По данным этих приборов принимается решение об установке умягчителя воды. Тестирование помогает определить не только качество воды, но и эффективность работы фильтров.
H2O из бассейна
Для обеззараживания воды в бассейне до сих пор иногда используется хлор. В этом случае приобретается фотометр с функцией определения хлора, его соединений и циануровой кислоты. Подойдет погружной фотометр SCUBA II.
Вместо хлора в частных бассейнах нередко применяется активный кислород. Его чрезмерная концентрация вредна для здоровья, поэтому приобретается прибор для измерения количества кислорода, растворенного в воде. Например, оксиметр Milwaukee Mw600.
Откуда берутся в воде?
Источник лабораторного появления этих соединений – довольно агрессивная по химическим свойствам хлороводородная кислота (HCl), легко вступающая в реакции с металлами, оксидами металлов, основаниями, солями других кислот. Более сложный вариант, – требующий серьезного нагревания и контакта металлов в свободном состоянии с ядовитыми газами – хлором (Cl2) и хлороводородом (HCl), – возможен, но в естественной среде маловероятен.
«Хлоридный фон» в запасниках рек, озер, невероятно соленых морей и океанов, подземных и наземных водоемов, ручейков и минеральных источников – естественное природное явление. В свободном виде хлориды чаще всего содержатся в различных минералах: бишофит, антрактицит, каломель, карналлит, галит, кераргирит. В местах природных залежей этих минералов хлоридов в ближайших водоемах особенно много. В сточные воды соли соляной кислоты попадают в результате активной деятельности человека.
Хлорирование – очистка вод «хлоркой»
Только неукоснительное соблюдение санитарных требований, предъявляемых к устройству и эксплуатации всех сооружений водопровода, позволяет гарантировать безопасность питьевой воды, подаваемой населению. Эти требования касаются и установок для хлорирования воды.
Влага – идеальная среда для развития бактерий, а хлор и его соединения успешно угнетают жизнедеятельность патогенной микрофлоры.
«Активный хлор» убивает бактерии, окисляя вещества протоплазмы клеток бактерий. Наиболее чувствительны к «активному хлору» возбудители холеры, брюшного тифа и дизентерии.
В России впервые хлорировали воду в Кронштадте – во время эпидемии холеры 1910 года. Первоначально хлорирование производили хлорной известью, а в 1917 году на водопроводной станции г. Ленинграда применили газообразный хлор.
Хлорирование – обязательная процедура в случае забора воды из поверхностных водоемов, а также подземных источников, когда бактериальные показатели пробы не соответствуют ГОСТ Р 51232-98 «Вода питьевая».
В резервуар с водой подается хлор в виде газа или раствора, затем происходит химическая реакция. В результате хлорирования качество обеззараживаемой жидкости сохраняется, а патогенные бактерии погибают.
Методические указания на фотометрическое определение хлора в воздухе (первый метод), МУ (Методические указания) от 18 апреля 1977 года №1644-77
УТВЕРЖДЕНЫ ЗаместителемГлавного государственного санитарного врача СССР А.И.Заиченко 18апреля 1977 года N 1644-77
I.Общая часть
1. Определение основанона иодкрахмальной реакции.
2. Предел обнаружения0,25 мкг хлора в анализируемом объеме раствора.
3. Предел обнаружения ввоздухе 0,5 мг/м (расчетная).
4. Определению мешаютбром, фтор и иод.
5. Предельно допустимаяконцентрация хлора в воздухе 1 мг/м.
II.Реактивы и аппаратура
6. Применяемые реактивы ирастворы.
Иод, 0,01 н. раствор(фиксанал), МРТУ 6-09-1678-64.
Стандартный раствор ссодержанием 0,0178 мг/мл иода готовят в день анализа в мерной колбеемкостью 50 мл путем разведения 0,7 мл 0,01 н. раствора иода2,5%-ным раствором иодистого калия. 1 мл стандартного растворасоответствует 5 мкг хлора.
Калий иодистый, ГОСТ 4232-65, 2,5%-ный раствор.
Ртуть двуиодистая, ГОСТ3206-46.
Крахмал растворимый,ГОСТ 10163-62, 0,2%-ный раствор.
2 г растворимого крахмала и 10 мг двуиодистой ртути растирают с 10мл воды. Полученную суспензию медленно вливают в 1 л кипящей воды.Кипячение продолжают пока раствор не станет прозрачным. Поохлаждении сливают в бутыль с пришлифованной пробкой; растворхранится до заметного помутнения.
Поглотительный раствор -смешивают 100 мл 2,5%-ный раствор иодида калия с 50 мл 0,2%-ногораствора крахмала и кипятят 2-3 мин. По охлаждении растворразбавляют водой до 500 мл.
Раствор можно хранить в течение 7 днейв бутыли с пришлифованной пробкой.
7. Применяемые посуда иприборы.
Аспирационноеустройство.
Поглотительные приборыЗайцева (см. рис.9).
Пробиркиколориметрические, плоскодонные из бесцветного стекла высотой 120мм, внутренним диаметром 15 мм.
Колбы мерные, ГОСТ 1770-74, вместимостью 1 л, 500 мл и50 мл.
Пипетки, ГОСТ 20292-74,вместимостью 1 и 5 мл с делениями на 0,01 и 0,1 мл.
Ступка с пестиком.